财联社5月3日讯(编辑 胡家荣)近年来,多家药企纷纷宣布“出海”,但其经过并不顺利,以和黄医药(00013)为例,该公司在2日晚间发布公告称,公司旗下索凡替尼药品遭美国食品药品监督管理局(FDA)拒绝,这引发该公司股价大幅下挫。
截止发稿,和黄医药(00013.HK)跌18.68%,报20.90港元。
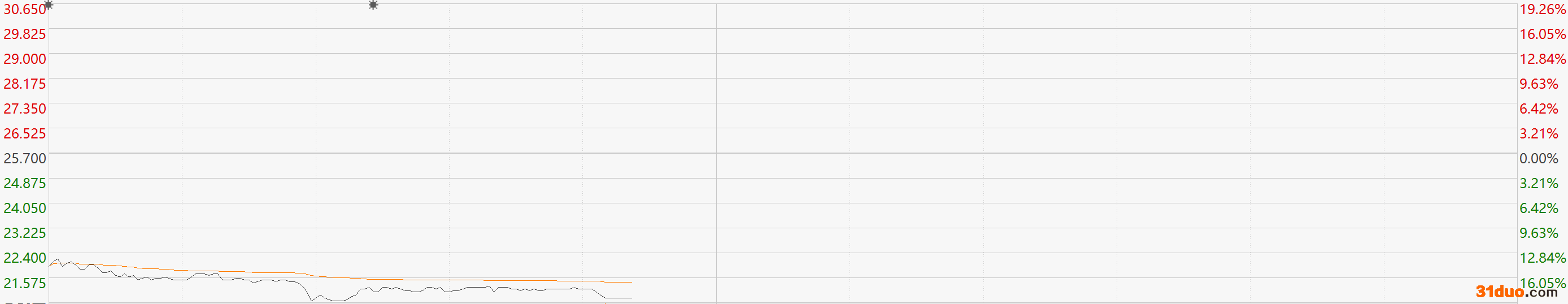
注:和黄医药当日走势
根据和黄医药公告,FDA已就索凡替尼用于治疗胰腺和非胰腺神经内分泌瘤的新药上市申请发出完整回复函。FDA认为,当前基于两项成功的中国III期研究以及一项美国桥接研究的数据包尚不足以支持药品现时于美国获批。

回复函中表明,需要纳入更多代表美国患者人群的国际多中心临床试验(MRCT)来支持美国获批。和黄医药正在与FDA合作,以评估下一步行动。
公告还指出,索凡替尼是一种具有抗血管生成和免疫调节双重活性的口服抑制剂,其安全性和疗效已在两项在中国晚期胰腺和非胰腺神经内分泌瘤患者中开展的随机双盲的III期研究(即SANET-ep和SANET-p研究)中得到证明,同时在美国开展的桥接研究结果也显示出与两项SANET研究人群中相似的安全性及疗效。
2020年5月,和黄医药在新药上市申请前会议上与FDA达成一致,索凡替尼用于治疗胰腺和非胰腺神经内分泌瘤患者的两项取得积极结果的中国III期研究,连同索凡替尼美国桥接研究的现有数据,可构成支持在美国提交新药上市申请的依据。FDA于2021年6月30日受理了索凡替尼提交的新药上市申请。
此外,美国证券业协会(SEC)在3月8日将百济神州(06160.HK)、百胜中国(09987.HK)、再鼎医药(02925.HK)、盛美半导体、和黄医药列入“预摘牌名单”。
(责任编辑:魏京婷)
中国经济网声明:股市资讯来源于合作媒体及机构,属作者个人观点,仅供投资者参考,并不构成投资建议。投资者据此操作,风险自担。
打开微信,点击底部的“发现”,使用 “扫一扫” 即可将网页分享到我的朋友圈。

